Автокатализ (от авто... и катализ), ускорение химической реакции одним из её продуктов. Пример А.: гидролиз этил-ацетата в водном растворе:
CH3COOC2H5 + H2O = CH3COOH + C2H5OH.
Продукт реакции — уксусная кислота CH3COOH и ион Н+, образующийся при её электролитической диссоциации, ускоряют реакцию. Скорость автокаталитической реакции вначале возрастает вследствие увеличения количества продукта, являющегося катализатором, а затем падает в результате израсходования исходных веществ. Поэтому зависимость степени превращения a от времени t описывается S-образной кривой (см. рис.). Реакция начинается благодаря присутствию в начальный момент некоторого малого количества продукта (затравка) или другого катализатора, или, наконец, за счёт медленной некаталитической реакции, происходящей параллельно каталитической. Если начальная концентрация катализатора и скорость некаталитической реакции весьма малы, то в течение некоторого времени, называемого периодом индукции, реакция настолько медленна, что практически не обнаруживается, и лишь по истечении этого времени становится заметной.
Автокаталитический характер имеют процессы образования новой фазы, протекающие на границе раздела фаз (такие, как конденсация пересыщенного пара, кристаллизация переохлаждённой жидкости, топохимические реакции), т. к. по мере увеличения количества новой фазы растет поверхность раздела. Цепные разветвленные реакции могут быть внешне весьма сходны с автокаталитическими. Отличие заключается в том, что ускорение реакции при разветвлении цепей вызвано накоплением активных промежуточных веществ, а не продуктов реакции (см. Цепные реакции).
Термин «А.» иногда применяют и в тех случаях, когда катализатором является одно из исходных веществ реакции.
М. И. Тёмкин.
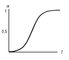
Автокаталитическая реакция первого порядка (по исходному веществу и продукту); начальная концентрация продукта равна 0,1% от начальной концентрации исходного вещества.