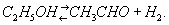
Гидрогенизация (от лат. hydrogenium — водород), гидрирование, каталитическая реакция присоединения водорода к простым веществам (элементам) или химическим соединениям. Обратная реакция — отщепление водорода от химических соединений — называется дегидрогенизацией (дегидрированием). Г. и дегидрогенизация — важные методы каталитического синтеза различных органических веществ, основанные на реакциях окислительно-восстановительного типа, связанных подвижным равновесием (см. Равновесие химическое). Примером может служить обратимое каталитическое превращение этилового спирта в ацетальдегид:
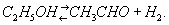
Повышение температуры и понижение давления H2 способствуют образованию ацетальдегида, а понижение температуры и повышение давления H2 — образованию этилового спирта; такое влияние условий типично для всех реакций Г. и дегидрогенизации. Катализаторами Г. и дегидрогенизации являются многие металлы (Fe, Ni, Со, Pt, Pd, Os и др.), окислы (NiO, CoO, Cr2O3, MoO2 и др.), а также сульфиды (WS2, MoS2, CrnSm).
Г. и дегидрогенизация широко используются в промышленности. Например, синтез такого важного продукта, как метиловый спирт, служащий сырьём для многих химических производств и растворителем, осуществляют Г. окиси углерода (CO + 2H2 ® CH3OH) на окисных цинк-хромовых катализаторах при 300—400°С и давлении водорода 20—30 Мн/м2 (200—300 кгс/см2). При другом составе катализаторов этим методом можно получать и высшие спирты. Г. жиров лежит в основе производства маргарина (см. Жиров гидрогенизация). В связи с возникновением производства таких материалов, как капрон, найлон и пр. (см. Полиамидные волокна), метод Г. стал широко применяться для получения промежуточных продуктов — циклогексанола из фенола, циклогексана из бензола, гексаметилендиамина из динитрила адипиновой кислоты (на никелевых катализаторах) и циклогексиламина из анилина (на кобальтсодержащих катализаторах).
Для облагораживания топлив, получаемых из сернистых нефтей, большое значение имеет гидроочистка (см. Очистка нефти) — Г. на алюмо-кобальт-молибденовом или вольфрамо-никелевом катализаторах, приводящая к разрушению органических сернистых соединений и удалению серы в виде H2S. Другой процесс облагораживания нефтепродуктов — гидрогенизация деструктивная (на вольфрамсульфидных и некоторых др. катализаторах) — приводит к увеличению выхода светлых и лёгких продуктов при переработке нефти. При Г. CO на различных катализаторах можно получать бензин, твёрдые парафины или кислородсодержащие органические соединения. Синтез неорганического вещества аммиака взаимодействием азота и водорода под высоким давлением также относится к Г. и является примером Г. простого вещества.
Один из простейших примеров дегидрогенизации — дегидрирование спиртов. Значительное количество ацетальдегида производится дегидрогенизацией гидролизного (получаемого из древесины) этилового спирта. Дегидрогенизация углеводородов является одной из основных реакций, протекающих на смешанных катализаторах в сложном процессе риформинга, который приводит к существенному улучшению качеств моторных топлив; эта реакция позволяет получать также различные ароматические углеводороды из нафтеновых и парафиновых (см. также Ароматизация нефтепродуктов).
Широкое применение дегидрогенизация нашла в производстве мономеров для синтеза каучуков и смол. Так, парафиновые углеводороды бутан и изопентан дегидрируются при 500—600°С на катализаторах, содержащих окись хрома, соответственно в бутилены и изопентен (изоамилен), которые, в свою очередь, дегидрируются на сложных катализаторах в диолефины — бутадиен и изопрен. В производстве полимеров стирола и его производных большое значение приобрела дегидрогенизация алкилароматических углеводородов — этилбензола в стирол, изопропилбензола в метилстирол и т.п.
Начало широкого изучения Г. было положено в 1897—1900 научными школами П. Сабатье во Франции и Н. Д. Зелинского в России. Основные закономерности Г. смесей органических соединений установил С. В. Лебедев. В области практического применения Г. крупные успехи были достигнуты уже в 1-й четверти 20 в. Ф. Габером (синтез аммиака), Ф. Бергиусом (Г. угля) и Г. Патаром (Франция; синтез метанола). Дегидрогенизацию спиртов открыл в 1886 М. Бертло. В 1901 Сабатье наблюдал наряду с др. превращениями углеводородов и их дегидрогенизацию. В чистом виде дегидрогенизацию углеводородов впервые удалось осуществить Н. Д. Зелинскому, разработавшему ряд избирательно действующих катализаторов. Большой вклад в развитие теории и практики Г. и дегидрогенизации внесли Б. А. Казанский, А. А. Баландин и их научной школы.
Лит.: Лебедеве. В., Жизнь и труды, Л., 1938; Зелинский Н. Д., Собр. трудов, т. 3 — Катализ, М., 1955; Долгов Б. Н., Катализ в органической химии, 2 изд., Л., 1959; Баландин А. А., Мультиплетная теория катализа, ч. 1—2, М., 1963—64; Юкельсон И. И., Технология основного органического синтеза, М., 1968; Bond G. С., Catalysis by metals, L. — N. Y., 1962; Ридил Э., Развитие представлений в области катализа, пер. с англ., М., 1971, гл. 6 и 7.
А. М. Рубинштейн.